碧云天生产的BeyoGold™ His-tag Purification Resin (耐变性剂型),即BeyoGold™ His-tag Purification Resin (Denaturant- resistant),是一种耐变性剂型的His标签蛋白纯化介质,俗称镍柱。本产品是一种新型的可以兼容尿素和盐酸胍等强蛋白变性剂,从而不仅可以在非变性条件下也可以在变性条件下简单、快速、高效并且高特异性地纯化His标签蛋白的纯化介质。
通常带有6个组氨酸标签的重组蛋白(6xHis-tagged recombinant protein)或带有6个以上连续组氨酸标签的重组蛋白,被称为His标签蛋白。蛋白样品溶液通过BeyoGold™ His-tag Purification Resin (耐变性剂型)时,重组蛋白His标签上的组氨酸残基能特异性地结合到BeyoGold™ His-tag Purification Resin (耐变性剂型)中的镍离子上,其它蛋白则不能被结合。洗涤后,His标签重组蛋白可在非变性条件下或者变性条件下被洗脱,从而被分离纯化。
本产品对His标签重组蛋白的亲和力强、选择性高、结合容量大,使用本产品可以获得高纯度的His标签重组蛋白,可用于简单、快速、高效地纯化细菌、哺乳动物细胞、昆虫及杆状病毒等多种表达系统中表达的His标签重组蛋白。纯化的蛋白可以用于结构和功能研究、抗体制备、蛋白与蛋白相互作用、蛋白与核酸相互作用等方面的研究。
本产品采用了一种高度交联的6%琼脂糖凝胶(Beyorose CL-6B,与Sepharose CL-6B性能基本一致)为基质,并使用了进一步优化的接臂和镍离子螯合技术,和目前市售的同类产品相比,非特异性蛋白结合显著降低。
本产品可以耐受8M尿素或6M盐酸胍,可用于非变性条件和变性条件下His标签蛋白的纯化。DTT、-巯基乙醇等还原剂会还原螯合结合的镍离子,而EDTA/EGTA等二价离子强螯合剂则会使本产品脱镍,因此在蛋白样品或者纯化过程所使用的溶液中不能含有还原剂和螯合剂。如需在强还原剂如DTT/-巯基乙醇或螯合剂EDTA/EGTA存在的条件下纯化蛋白,推荐使用碧云天的耐受还原剂和螯合剂的P2210/P2218/P2220 BeyoGold™ His-tag Purification Resin (耐还原螯合型)。
本产品已经螯合了镍离子,呈蓝绿色,凝胶的颗粒直径为45-165μm。可耐受的最大压力为0.025MPa,约合5.8psi。采用固定流速进行蛋白纯化时的推荐流速为0.5ml/min。
本产品可以高容量、高特异性地结合His标签蛋白。最大蛋白结合量约为25-35mg蛋白(分子量为55kD的蛋白)/毫升凝胶。实际使用时的最大结合量主要取决于待纯化的His标签重组蛋白的分子量大小,分子量越大则最大结合容量越大,分子量越小则最大结合容量越小。但对于分子量相同的蛋白,也会因为蛋白本身特性的不同,结合的最大容量也会有所不同。
本产品储存在20%乙醇中。本产品包装体积中50%为凝胶,例如10ml总体积中5ml为凝胶,5ml为液体。使用时宜把凝胶充分重悬后再吸取。
每10ml包装的本产品最多可纯化100-200mg带有His标签的重组蛋白(分子量为55kD的蛋白),分子量更大的蛋白结合容量会更大一些。
包装清单:
| 产品编号 | 产品名称 | 包装 |
| P2233-10ml | BeyoGold™ His-tag Purification Resin (耐变性剂型) | 10ml |
| P2233-100ml | BeyoGold™ His-tag Purification Resin (耐变性剂型) | 100ml |
| P2233-1000ml | BeyoGold™ His-tag Purification Resin (耐变性剂型) | 100ml×10 |
| - | 说明书 | 1份 |
保存条件:
4℃保存,至少一年有效。
注意事项:
请勿在-20℃或更低温度冷冻保存本产品。
本产品使用过程中,缓冲试剂如Tris、HEPES、MOPS等的浓度不宜超过100mM,SDS和sarkosyl的浓度不宜超过0.3%,Triton X-100、Tween-20、NP-40的浓度不宜超过2%,脱氧胆酸钠、CHAPS的浓度不宜超过1%,组氨酸浓度不宜超过20mM,钙离子浓度不宜超过5mM,钠离子和镁离子浓度可以高达2M,盐酸胍浓度可以高达6M,尿素浓度可以高达8M,甘油浓度可以高达50%。本产品不能耐受还原剂、螯合剂和强酸强碱。其它未提及试剂的兼容性可以参考上述试剂,但还有待实验验证。
保存和纯化过程中应始终保持凝胶湿润。
碧云天有多种不同容量的亲和层析柱空柱管(FCL01/FCL03/FCL06/FCL12/FCL30/FCL60),可以和本产品配合使用。
若离心不能完全除去蛋白样品中的不溶物,可以将样品溶液用0.45µm的滤膜过滤。
蛋白样品收集后宜尽快完成纯化工作,并应始终放置在4℃或冰浴,以减缓蛋白降解。为有效抑制蛋白降解,可以在裂解液中添加适量的蛋白酶抑制剂混合物,例如碧云天的P1030/P1031 蛋白酶抑制剂混合物(His-Tag蛋白纯化用, 100X)。
若使用本说明书提供的条件无法达到理想的纯化效果,可尝试改变洗涤液和洗脱液中咪唑的浓度和(或)pH,以达到最优效果。
如果目的蛋白纯化必须使用螯合剂或还原剂,推荐使用碧云天生产的P2210/P2218/P2220 BeyoGold™ His-tag Purification Resin (耐还原螯合型)。
本产品仅限于专业人员的科学研究用,不得用于临床诊断或治疗,不得用于食品或药品,不得存放于普通住宅内。
为了您的安全和健康,请穿实验服并戴一次性手套操作。
使用说明:
对于用镍柱纯化大肠杆菌中His标签蛋白比较熟悉的使用者可以直接参考“6. 简化的操作流程”。否则请参考如下详细内容:
如下以最常见的大肠杆菌中表达纯化His标签重组蛋白为例,说明本产品的使用方法。在其它体系中表达时,请参考该表达体系的相关使用说明,并借鉴大肠杆菌中纯化His标签重组蛋白的使用说明。
1.大肠杆菌中His标签重组蛋白的诱导表达:
如下以最常用的IPTG诱导表达系统给予说明,诱导表达条件的优化请参照所使用的诱导表达体系的详细说明。其它诱导表达系统请参考适当的使用说明进行。
a.挑取表达His标签重组蛋白的单克隆,接种到3ml或10-20ml含适当抗生素的LB培养液中,培养过夜。
b.按照1:20的比例取培养过夜的菌液,接种到预热至37℃并含适当抗生素的LB培养液中。例如取5ml培养过夜的菌液接种到100ml预热至37℃并含适当抗生素的LB培养液中。具体的培养体积视需要纯化的蛋白量而定,初步的鉴定培养3-10ml即可;常规的表达纯化,通常可考虑培养100-200ml;制备型的纯化,培养体积可以达到1L或更大。如果希望取得更好的表达效果,建议按照1:100的比例接种过夜培养的菌液,但后续培养至相应的OD值需要更长的时间。
c.37℃常规培养约30-60min或更长时间,至菌液的OD600达到0.5-0.7,并且OD600最好接近0.6。
d.加入IPTG至终浓度为1mM,继续培养4-5小时。
注:可以在加入IPTG前取出少量菌液同样培养4-5小时后作为未诱导的对照,也可以在加入IPTG前直接取出少量菌液作为未诱导的对照。对于特定蛋白的诱导表达,最佳的IPTG浓度、诱导温度、和诱导时间需要通过实验确定。
e.收集菌液至离心管中,4℃ 4,000g离心20min或4℃ 15,000g离心1min,弃上清,收集沉淀。随后即可进入细菌裂解步骤,也可以在-20℃或-80℃冻存备用。冷冻保存的菌体使用前需置于冰上解冻15min。
2.非变性条件下His标签蛋白的小量纯化:
本方法常用于小量样品的快速分析和鉴定,为后续大量制备打下基础。
a.接步骤1(e),离心收集1ml菌液的细菌沉淀并弃上清,加入100µl非变性裂解液,将细菌沉淀充分重悬于裂解液中,可进行轻微的vortex(尽量避免产生气泡)。
注:根据His标签重组蛋白表达的丰度,菌液和裂解液的体积比可以在25:1-5:1范围内适当调整。表达丰度非常高时,每毫升菌液沉淀可以加入200µl裂解液;表达丰度非常低时,每毫升菌液沉淀可以加入40µl裂解液。相关溶液的配制方法附后。本非变性裂解液可以确保裂解绝大多数可溶性蛋白和包涵体蛋白,裂解后可以直接用于SDS-PAGE。如有必要,可以在裂解细菌之前,在裂解液中添加适量的蛋白酶抑制剂混合物,例如碧云天的P1030/P1031 蛋白酶抑制剂混合物(His-Tag蛋白纯化用, 100X)。
b.加入溶菌酶至1mg/ml并轻轻混匀,尽量避免产生气泡,冰水浴或冰上放置30min。
注:如果没有溶菌酶,也可以直接冰上超声裂解细菌,随后进入步骤2d。超声功率200-300W,每次超声处理10s,每次间隔10s,共超声处理6次。具体超声处理的方式须根据特定型号的超声仪器自行摸索和优化。
c.轻轻vortex数下,以充分裂解细菌,尽量避免产生气泡。
d.4℃离心(15000g×10min),取10µl上清留样作后续检测用,收集余下上清至一新的洁净离心管中。
e.加入20µl混合均匀的50% BeyoGold™ His-tag Purification Resin (耐变性剂型),4℃在摇床上缓慢摇动30min,以充分结合带His标签的目的蛋白。
注:缓慢摇动30min已经可以确保蛋白充分结合,但可以根据时间安排的需要缓慢摇动更长时间甚至缓慢摇动过夜。经测试,直接使用50% BeyoGold™ His-tag Purification Resin (耐变性剂型)也能获得良好的纯化效果。但如果希望获得更高的标签蛋白得率,可以事先用一个柱体积的非变性裂解液平衡BeyoGold™ His-tag Purification Resin (耐变性剂型) 2-3次。平衡后,视不同的待纯化蛋白而定,待纯化蛋白的得率有可能会提高约5-20%左右。
f.4℃离心(1000g×10s)沉淀凝胶,取20µl上清留样作后续检测用,其余上清弃去。
g.加入100µl非变性洗涤液重悬凝胶,4℃离心(1000g×10s),取20µl上清留样作后续检测用,其余上清弃去。
h.重复步骤g,再进行一次洗涤。
i.加入20µl非变性洗脱液,轻轻重悬凝胶。4℃离心(1000g×10s),收集上清及凝胶。上清即为纯化获得的带有His标签的目的蛋白。
j.重复步骤i两次。共洗脱收集约60µl纯化的蛋白样品。
3.非变性条件下His标签蛋白的大量纯化:
a.接步骤1(e),对于新鲜的或解冻的细菌沉淀,按照每升(指步骤1中培养时的体积)表达菌中加入80ml非变性裂解液的比例加入裂解液,充分重悬菌体。如有必要,可以在裂解细菌之前,在裂解液中添加适量的蛋白酶抑制剂混合物,例如碧云天的P1030/P1031 蛋白酶抑制剂混合物(His-Tag蛋白纯化用, 100X)。
b.加入溶菌酶至终浓度为1mg/ml并混匀,冰水浴或冰上放置30min。
注:如果没有溶菌酶,也可以直接进入步骤3c。
c.冰上超声裂解细菌。超声功率200-300W,每次超声处理10s,每次间隔10s,共超声处理6次。如果未经溶菌酶处理,推荐每次超声处理2s,每次间隔2s,共超声处理15-30min。
注:具体超声处理的方式须根据特定型号的超声仪器自行摸索和优化。
d.(可选做)如果超声处理后裂解液非常粘稠,可以加入RNase A至10µg/ml及DNase I至5µg/ml,冰上放置10-15min。或者也可以使用适当的装好了较细针头的注射器,反复抽吸数次,以剪切粘稠的基因组DNA等。
e.4℃ 10,000g离心20-30min,收集细菌裂解液上清并置于冰水浴或冰上。可以取20µl上清留作后续检测用。
注:上清必须保持澄清,即不含任何不溶物,才能进行下一步的纯化。上清中如果混有不溶性杂质会严重影响后续纯化获得蛋白的纯度。
f.按照每4ml细菌裂解液上清加入1ml混合均匀的50% BeyoGold™ His-tag Purification Resin (耐变性剂型)的比例(4:1),混合细菌裂解液上清和50% BeyoGold™ His-tag Purification Resin (耐变性剂型)。4℃在侧摆摇床或水平摇床上缓慢摇动60min。
g.将裂解液和BeyoGold™ His-tag Purification Resin (耐变性剂型)的混合物装入适当的空柱管中,如碧云天的亲和层析柱空柱管。
注:也可先装柱,用1倍柱体积的非变性裂解液平衡后加入细菌裂解液上清,后续可以把穿流液收集后重复上柱3-5次以充分结合目的蛋白。先混合后装柱的方式操作起来相对麻烦一些,但更有利于带有His标签重组蛋白与镍柱的充分结合,特别是当His标签被蛋白本身部分遮挡或His标签重组蛋白浓度很低时与镍柱的结合效率会高一些。
h.将纯化柱底部的盖子打开,在重力作用下使柱内液体流出,收集约20µl穿流液作后续分析用。
i.洗柱5次,每次加入1-2个柱体积的非变性洗涤液,每次均收集约20μl穿柱的洗涤液用于后续的分析检测用。例如1ml混合均匀的50% BeyoGold™ His-tag Purification Resin (耐变性剂型)装柱后的柱体积为0.5ml,即1ml混合均匀的50% BeyoGold™ His-tag Purification Resin (耐变性剂型)装柱后每次洗柱的洗涤液体积为0.5ml。洗柱及下一步洗脱过程中可以用Bradford法(P0006)简单快速地检测每次洗涤液和洗脱液中的蛋白含量,从而考虑增加或减少洗涤和洗脱的次数。
注:如果出现后续获得蛋白纯度不够高的情况,可以再增加洗柱次数2-3次,或者在非变性洗涤液洗涤之前用非变性裂解液洗柱3-5次,每次1-2个柱体积。
j.洗脱目的蛋白5-10次,每次用一个柱体积的非变性洗脱液。将每次的洗脱液分别收集到不同的离心管中。收集获得的洗脱液即为纯化的His标签蛋白样品。蛋白纯化效果可以参考图1。
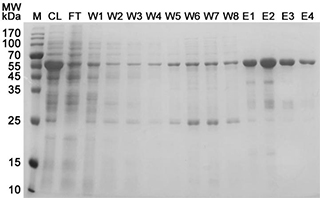
图1. 非变性条件下His标签重组蛋白纯化效果图。M: marker (P0076); CL:细菌裂解液(cell lysate);FT:上样穿流液(flow through);W1-W3:非变性裂解液洗涤1-3 (wash 1-3);W4-W8:非变性洗涤液(非变性裂解液添加20mM咪唑)洗涤4-8;E1-E4:洗脱液(非变性裂解液添加250mM咪唑)洗脱1-4 (elution 1-4)。注:实际的电泳结果会因样品、上样量等的不同而有所不同。
4.变性条件下His标签蛋白的小量纯化:
本方法常用于小量样品的快速分析和鉴定,为后续大量制备打下基础。
a.接步骤1(e),离心收集1ml菌液的细菌沉淀并弃上清,加入100μl变性裂解液,将细菌沉淀充分重悬于裂解液中,可进行轻微的vortex(尽量避免产生气泡)。
注:根据His标签重组蛋白表达的丰度,菌液和裂解液的体积比可以在25:1-5:1范围内适当调整。表达丰度非常高时,每毫升菌液沉淀可以加入200μl裂解液;表达丰度非常低时,每毫升菌液沉淀可以加入40μl裂解液。相关溶液的配制方法附后。本变性裂解液可以确保裂解绝大多数可溶性蛋白和包涵体蛋白,含尿素裂解液裂解后可以直接用于SDS-PAGE,含盐酸胍的裂解液裂解后需透析除去盐酸胍才可用于SDS-PAGE。
b.冰上超声裂解细菌。超声功率200-300W,每次超声处理10s,每次间隔10s,共超声处理6次。具体超声处理的方式须根据特定型号的超声仪器自行摸索和优化。
c.4℃离心(15000g×10min),取10μl上清留样作后续检测用,收集余下上清至一新的洁净离心管中。
d.加入20μl混合均匀的50% BeyoGold™ His-tag Purification Resin (耐变性剂型),4℃在摇床上缓慢摇动30min,以充分结合带His标签的目的蛋白。
注:缓慢摇动30min已经可以确保蛋白充分结合,但可以根据时间安排的需要缓慢摇动更长时间甚至缓慢摇动过夜。经测试,直接使用50% BeyoGold™ His-tag Purification Resin (耐变性剂型)也能获得良好的纯化效果。但如果希望获得更高的标签蛋白得率,可以事先用一个柱体积的变性裂解液平衡BeyoGold™ His-tag Purification Resin (耐变性剂型)2-3次。平衡后,视不同的待纯化蛋白而定,待纯化蛋白的得率有可能会提高约5-20%左右。
e.4℃离心(1000g×10s)沉淀凝胶,取20μl上清留样作后续检测用,其余上清弃去。
f.加入50-100μl变性裂解液重悬凝胶,4℃离心(1000g×10s),取20μl上清留样作后续检测用,其余上清弃去。
g.重复步骤f,再进行一次洗涤。
h.加入20μl变性洗脱液,轻轻重悬凝胶。4℃离心(1000g×10s),收集上清及凝胶。上清即为纯化的带有His标签的目的蛋白。
i.重复步骤h两次。共洗脱收集约60μl纯化的蛋白样品。
5.变性条件下His标签蛋白的大量纯化:
接步骤1(e),对于新鲜的或解冻的细菌沉淀,按照每1L表达菌加入80ml变性裂解液的比例加入裂解液,充分重悬菌体。
a.冰上超声裂解细菌。超声功率200-300W,每次超声处理2s,每次间隔2s,共超声处理15-30min。
注:具体超声处理的方式须根据特定型号的超声仪器自行摸索和优化。
b.(可选做)如果超声处理后裂解液非常粘稠,可以使用适当的装好了较细针头的注射器,反复抽吸数次,以剪切粘稠的基因组DNA等。
c.4℃ 10,000g离心20-30min,收集细菌裂解液上清并置于冰水浴或冰上。可以取20μl上清留作后续检测用。
注:上清必须保持澄清,即不含任何不溶物,才能进行下一步的纯化。上清中如果混有不溶性杂质会严重影响后续纯化获得蛋白的纯度。
d.取适量混合均匀的50% BeyoGold™ His-tag Purification Resin (耐变性剂型),4℃离心(1000g×10s)弃去储存液,向凝胶中加入一个柱体积的变性裂解液混匀以平衡凝胶,4℃离心(1000g×10s)弃去液体,再重复平衡1-2次,弃去液体。
e.按照每0.5ml凝胶(相当于1ml 50%的凝胶)中加入4ml细菌裂解液上清的比例(1:8),混合BeyoGold™ His-tag Purification Resin (耐变性剂型)和细菌裂解液上清。4℃在侧摆摇床或水平摇床上缓慢摇动60min。
f.将裂解液和BeyoGold™ His-tag Purification Resin (耐变性剂型)的混合物装入适当的空柱管中,如碧云天的亲和层析柱空柱管。
注:也可先装柱,用1倍柱体积的变性裂解液平衡后加入细菌裂解液上清,后续可以把穿流液收集后重复上柱3-5次以充分结合目的蛋白。先混合后装柱的方式操作起来相对麻烦一些,但更有利于带有His标签重组蛋白与镍柱的充分结合。
g.将纯化柱底部的盖子打开,在重力作用下使柱内液体流出,收集约20µl穿流液作后续分析用。
h.洗柱5次,每次加入1-2个柱体积的变性裂解液,每次均收集约20μl穿柱的裂解液用于后续的分析检测用。例如1ml混合均匀的50% BeyoGold™ His-tag Purification Resin (耐变性剂型)装柱后的柱体积为0.5ml,即1ml混合均匀的50% BeyoGold™ His-tag Purification Resin (耐变性剂型)装柱后每次洗柱的裂解液体积为0.5-1ml。洗柱及下一步洗脱过程中可以用Bradford法(P0006)简单快速地检测每次洗涤液和洗脱液中的蛋白含量,从而考虑增加或减少洗涤和洗脱的次数。
注:如果出现后续获得蛋白纯度不够高的情况,可以再增加洗柱次数2-3次。
i.再次洗柱5次,每次加入1-2个柱体积的变性洗涤液,每次均收集约20μl穿柱的洗涤液用于后续的分析检测用。
注:如果出现后续获得蛋白纯度不够高的情况,可以再增加洗柱次数2-3次。
j.洗脱目的蛋白5-10次,每次用一个柱体积的变性洗脱液。将每次的洗脱液分别收集到不同的离心管中。收集获得的洗脱液即为纯化的His标签蛋白样品。蛋白纯化效果可以参考图2及图3。
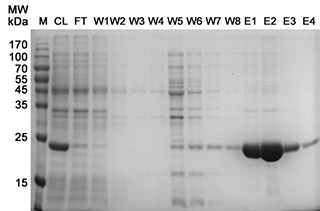
图2. 8M尿素变性条件下His标签重组蛋白纯化效果图(所用溶液均含有8M尿素)。M:marker (碧云天P0076);CL:细菌裂解液(cell lysate);FT:上样穿流液(flow through);W1-W3:变性裂解液洗涤1-3;W4-W8:变性洗涤液(变性裂解液添加20mM咪唑)洗涤;E1-E4:洗脱液1-4 (变性裂解液添加250mM咪唑)。注:实际的电泳结果会因样品、上样量等的不同而有所不同。
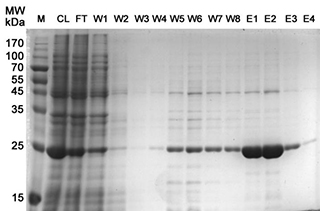
图3. 6M盐酸胍变性条件下His标签重组蛋白纯化效果图(所用溶液均含有6M盐酸胍,各样品电泳前通过透析除去盐酸胍)。M:marker (碧云天P0076);CL:细菌裂解液(cell lysate);FT:上样穿流液(flow through);W1-W3:变性裂解液洗涤1-3;W4-W8:变性洗涤液(变性裂解液添加20mM咪唑)洗涤;E1-E4:变性洗脱液1-4 (变性裂解液添加250mM咪唑)。注:实际的电泳结果会因样品、上样量等的不同而有所不同。
6.简化的操作流程:
a.细菌中的目的蛋白诱导表达后,离心沉淀细菌。
b.按照每克细菌沉淀湿重加入2-5ml裂解液的比例加入裂解液,可添加适量蛋白酶抑制剂(如碧云天的P1030/P1031),充分重悬细菌。
注:裂解液中咪唑浓度不宜超过20mM,通常0-10mM即可。本产品兼容Tris裂解液体系(参见后附的相关溶液配制方法)及NaH2PO4裂解液体系(50mM NaH2PO4, 300mM NaCl, pH 8.0)。
c.超声或其它适当方法裂解细菌,离心取上清。
d.BeyoGold™ His-tag Purification Resin (耐变性剂型)装柱,1倍柱体积裂解液平衡纯化柱2-3次。
e.步骤6c中的上清上柱。
注:上清上柱是可以收集穿流液并重复上柱3-5次,以充分结合His标签蛋白。
f.用一倍柱体积的洗涤液洗柱5次。
注:洗涤液中咪唑浓度不宜超过20mM,通常10-20mM即可,首次实验推荐使用含20mM咪唑的洗涤液。如果发现效果欠佳,可以根据实际情况上调或下调咪唑的浓度。如果洗脱不干净,可以增加洗涤次数或者增加洗涤液中的咪唑浓度。
g.用一倍柱体积的洗脱液洗脱5-10次。
7.BeyoGold™ His-tag Purification Resin (耐变性剂型)的再生
使用过的BeyoGold™ His-tag Purification Resin (耐变性剂型)可以通过如下方法再生后继续使用。但再生的BeyoGold™ His-tag Purification Resin (耐变性剂型)通常宜仅用于相同蛋白的纯化,并且最多再生3-4次。一次或多次再生后,BeyoGold™ His-tag Purification Resin (耐变性剂型)的蛋白结合能力会有所下降,并且非特异性结合也会升高。
如有需要,可以参考如下步骤进行镍柱的再生:
a.加入5倍柱体积的去离子水洗柱一次。
b.加入1倍柱体积的25%、50%、75%乙醇各洗柱一次。
c.加入5倍柱体积的100%乙醇洗柱一次。
d.加入1倍柱体积的75%、50%、25%乙醇各洗柱一次。
e.加入2倍柱体积的去离子水洗柱一次。
f.加入2倍柱体积的200mM EDTA (pH 8.0),洗柱一次。
g.加入5倍柱体积的去离子水洗柱一次。
h.加入3倍柱体积的50mM NiSO4洗柱一次。
i.加入3倍柱体积的非变性裂解液洗柱一次。
j.加入3倍柱体积的去离子水洗柱一次。
k.随后把BeyoGold™ His-tag Purification Resin (耐变性剂型)存放在20%乙醇中,4ºC保存,后续即可用于相同蛋白的纯化。
常见问题:
如果纯化不成功,可以对纯化过程中收集的每个组分进行SDS-PAGE电泳检测,分析其原因。
1.蛋白无法与BeyoGold™ His-tag Purification Resin (耐变性剂型)结合
a.测序检查基因序列的读码框是否正确。
b.尝试将标签加在蛋白的另一端。
c.增加BeyoGold™ His-tag Purification Resin (耐变性剂型)与蛋白结合时间(如4℃过夜)。
d.如果使用预装柱,可收集裂解液上柱后的穿流液并多次重复上柱。
e.检查所有缓冲液和溶液的pH值是否正确。
f.确认体系中所用各种试剂的浓度在镍柱的耐受范围以内。
g.自行配制裂解液,降低裂解液中的咪唑浓度。
2.目的蛋白被洗涤液洗脱
a.自行配制洗涤液,降低洗涤液中的咪唑浓度或者稍微提高其pH值。
b.检查洗涤液的pH和成分。
c.确认洗涤液中各种试剂的浓度在耐受范围内。
3.蛋白在纯化过程中形成沉淀
a.将纯化温度控制在室温。
b.加入去垢剂,如0.1% Triton X-100或者Tween-20。
4.蛋白无法洗脱
a.用梯度pH及咪唑洗脱,确定最优洗脱条件。
5.目的蛋白与其它蛋白共同洗脱
a.提高裂解液和洗涤液中的咪唑浓度。
b.降低BeyoGold™ His-tag Purification Resin (耐变性剂型)的使用量。
c.增加盐或者去垢剂浓度,或者向洗涤液中加入乙醇或甘油以降低非特异相互作用。
d.检查基因内部是否含有起始密码子(C端标记蛋白)或者提前终止位点(N端标记蛋白)。
相关溶液配制方法:
| 1. | 非变性裂解液(1L): | |
| 50 mM Tris | 6.06 g Tris (MW 121.14 g/mol) | |
| 500 mM NaCl | 29.22 g NaCl (MW 58.44 g/mol) | |
| 用盐酸调节pH值至7.5。 | ||
| 2. | 非变性洗涤液(1L): | |
| 50 mM Tris | 6.06 g Tris (MW 121.14 g/mol) | |
| 500 mM NaCl | 29.22 g NaCl (MW 58.44 g/mol) | |
| 10-20 mM imidazole | 0.68-1.36 g imidazole (MW 68.08 g/mol) | |
| 用盐酸调节pH值至7.5。 | ||
| 3. | 非变性洗脱液(1L): | |
| 50 mM Tris | 6.06 g Tris (MW 121.14 g/mol) | |
| 500 mM NaCl | 29.22 g NaCl (MW 58.44 g/mol) | |
| 250 mM imidazole | 17.02 g imidazole (MW 68.08 g/mol) | |
| 用盐酸调节pH值至7.5。 | ||
| 4. | 变性裂解液(1L): | |
| 50 mM Tris | 6.06 g Tris (MW 121.14 g/mol) | |
| 500 mM NaCl | 29.22 g NaCl (MW 58.44 g/mol) | |
| 8M 尿素/6M 盐酸胍 | 480.48 g尿素(MW 60.06 g/mol)/573.18 g盐酸胍(MW 95.53 g/mol) | |
| 用盐酸调节pH值至7.5。 | ||
| 5. | 变性洗涤液(1L): | |
| 50 mM Tris | 6.06 g Tris (MW 121.14 g/mol) | |
| 500 mM NaCl | 29.22 g NaCl (MW 58.44 g/mol) | |
| 8M 尿素/6M 盐酸胍 | 480.48 g尿素(MW 60.06 g/mol)/573.18 g盐酸胍(MW 95.53 g/mol) | |
| 10-20 mM imidazole | 0.68-1.36 g imidazole (MW 68.08 g/mol) | |
| 用盐酸调节pH值至7.5。 | ||
| 6. | 变性洗脱液(1L): | |
| 50 mM Tris | 6.06 g Tris (MW 121.14 g/mol) | |
| 500 mM NaCl | 29.22 g NaCl (MW 58.44 g/mol) | |
| 8M 尿素/6M 盐酸胍 | 480.48 g尿素(MW 60.06 g/mol)/573.18 g盐酸胍(MW 95.53 g/mol) | |
| 250 mM imidazole | 17.02 g imidazole (MW 68.08 g/mol) | |
| 用盐酸调节pH值至7.5。 |
相关产品:
| 产品编号 | 产品名称 | 包装 |
| P2210 | BeyoGold™ His-tag Purification Resin (耐还原螯合型) | 10ml |
| P2218 | BeyoGold™ His-tag Purification Resin (耐还原螯合型) | 100ml |
| P2220 | BeyoGold™ His-tag Purification Resin (耐还原螯合型) | 1000ml |
| P2226 | His标签蛋白纯化试剂盒(耐还原螯合型) | 10ml |
| P2229S | His标签蛋白纯化试剂盒(耐变性剂型) | 10ml |
| P2233-10ml | BeyoGold™ His-tag Purification Resin (耐变性剂型) | 10ml |
| P2233-100ml | BeyoGold™ His-tag Purification Resin (耐变性剂型) | 100ml |
| P2233-1000ml | BeyoGold™ His-tag Purification Resin (耐变性剂型) | 1000ml |
| P2250 | BeyoGold™ GST-tag Purification Resin | 1ml |
| P2251 | BeyoGold™ GST-tag Purification Resin | 10ml |
| P2253 | BeyoGold™ GST-tag Purification Resin | 100ml |
| P2255 | BeyoGold™ GST-tag Purification Resin | 1000ml |
| P2262 | BeyoGold™ GST-tag Purification Resin | 10ml |
| P1030 | 蛋白酶抑制剂混合物(His-Tag蛋白纯化用, 100X) | 1ml |
| P1031 | 蛋白酶抑制剂混合物(His-Tag蛋白纯化用, 100X) | 5ml |
| FCL01 | 亲和层析柱空柱管(1毫升) | 20套/包 |
| FCL03 | 亲和层析柱空柱管(3毫升) | 20套/包 |
| FCL06 | 亲和层析柱空柱管(6毫升) | 20套/包 |
| FCL12 | 亲和层析柱空柱管(12毫升) | 20套/包 |
| FCL30 | 亲和层析柱空柱管(30毫升) | 10套/包 |
| FCL60 | 亲和层析柱空柱管(60毫升) | 10套/包 |
| FCL108 | 离心空柱管(2毫升, 5微米孔径) | 50套/包 |
| FCL122 | 离心空柱管(2毫升, 20微米孔径) | 50套/包 |